查詢時(shí)請注意選擇相應(yīng)的產(chǎn)品編號
| 共價(jià)鍵的特征共價(jià)鍵具有飽和性 | |||
|---|---|---|---|
|
共價(jià)鍵是化學(xué)鍵中重要的一類,包括:極性鍵、非極性鍵、配位鍵、單鍵、雙鍵、叁鍵、σ鍵、π鍵等類別。共價(jià)鍵之一原子間通過共用電子對(電子云重疊)所形成的化學(xué)鍵叫做共價(jià)鍵。共價(jià)鍵之二原子間通過共用電子對(電子云重疊)所形成的化學(xué)鍵叫做共價(jià)鍵。共價(jià)鍵又稱原子鍵。
同種原子間形成的共價(jià)鍵,共用電子對不偏向任何一個(gè)原子,成鍵原子都不顯電性,這種鍵稱為非極性鍵。例如H2、Cl2、N2等,在化合物分子中,不同原子間形成的共價(jià)鍵,由于不同原子的電負(fù)性不同,共用電子對偏向電負(fù)性大的原子,電負(fù)性大的原子就帶部分負(fù)電荷,電負(fù)性小的原子就帶部分正電荷,這樣的鍵稱為極性鍵。
同種非金屬原子之間,或不同種非金屬原子之間成鍵時(shí),一般都是共價(jià)鍵。在形成共價(jià)鍵時(shí),當(dāng)自旋方向相反的未成對電子的原子相互接近時(shí),兩個(gè)核間電子云密度較大,即共用電子對屬成鍵的兩原子共有,圍繞兩個(gè)核運(yùn)動(dòng),受兩核吸引,在兩核間電子云重疊。
要形成穩(wěn)定的共價(jià)鍵,必須盡可能使電子云重疊程度大一些,我們知道,除了s電子以外,其它電子云都是有空間取向的,在成鍵時(shí),要盡可能沿著電子云密度最大的方向發(fā)生重疊。例如H2O中,氫原子的1s電子云沿著氧原子的2Px、2Py電子云的空間伸展方向的重疊,才能達(dá)到電子云重疊程度最大,形成穩(wěn)定的共價(jià)鍵,因此共價(jià)鍵具有方向性。元素的原子形成共價(jià)鍵時(shí),當(dāng)一個(gè)原子的所有未成對電子和另一些原子中自旋方向相反的未成對電子配對成鍵后,就不再跟其它原子的未成對電子配對成鍵。例如H2O分子中,O原子有兩個(gè)未成對電子,它只能跟兩個(gè)H原子的未成對電子配對,因此,共價(jià)鍵具有飽和性。
原子在形成共價(jià)分子時(shí)所形成的共價(jià)鍵數(shù)目,取決于它所具有的未成對電子的數(shù)目。因此,一個(gè)原子有幾個(gè)未成對電子(包括激發(fā)后形成的未成對電子),便可與幾個(gè)自旋方向相反的未成對電子配對成鍵。此為共價(jià)鍵的飽和性。兩個(gè)氫原子通過自旋方向相反的1s電子配對形成H-H單鍵結(jié)合成H2分子后,就不能再與第三個(gè)H原子的未成對電子配對了。氮原子有三個(gè)未成對電子,可與三個(gè)氫原子的自旋方向相反的未成對電子配對形成三個(gè)共價(jià)單鍵,結(jié)合成NH3。⑵共價(jià)鍵的方向性
根據(jù)原子軌道最大重疊原理,在形成共價(jià)鍵時(shí),原子間總是盡可能沿著原子軌道最大重疊的方向成鍵。軌道重疊越多,電子在兩核間的概率密度越大,形成的共價(jià)鍵就越穩(wěn)定。除s軌道呈球形對稱外,p、d、f軌道在空間都有一定的伸展方向。在成鍵時(shí)為了達(dá)到原子軌道的最大程度重疊,形成的共價(jià)鍵必然會有一定的方向性。
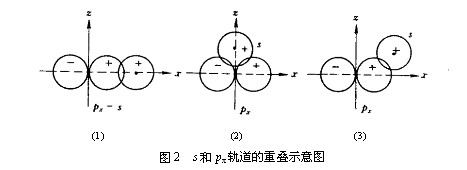
例如氫與氯結(jié)合形成HCl分子時(shí),氫原子的1s電子與氯原子的一個(gè)未成對電子(設(shè)處于3px軌道上)配對成鍵時(shí)有三種重疊方式。只有H原子的1s原子軌道沿著x軸的方向向Cl原子的3px軌道接近,才能達(dá)到最大的重疊,形成穩(wěn)定的共價(jià)鍵(圖2(1))。
圖2所示的s原子軌道接近px軌道的方式中,原子軌道同號重疊與異號重疊部分相等,正好相互抵消,這種重疊為無效重疊。故氫與氯在這個(gè)方向上不能結(jié)合。
圖2(3)所示的接近方向中,二原子軌道同號部分重疊較(1)為少,結(jié)合較不穩(wěn)定,氫原子有移向x軸的傾向。共價(jià)鍵的方向性決定了共價(jià)分子具有一定的空間構(gòu)型。
總結(jié):共價(jià)鍵有飽和性,成單電子的數(shù)目就是成鍵數(shù)目; 共價(jià)鍵有方向性,沿軌道方向重疊可產(chǎn)生最大重疊,形成的鍵最穩(wěn)定;在所有軌道中只有 s 軌道無方向性,只有 s 軌道之間形成的鍵無方向性~!
共價(jià)鍵的穩(wěn)定性首先與參與鍵的原子有關(guān),原子間的電負(fù)性差越大形成的共價(jià)鍵一般越穩(wěn)定;原子的原子半徑越小形成的共價(jià)鍵也越穩(wěn)定。還與原子參與組合的價(jià)軌道有關(guān)(對稱性), σ 對稱性穩(wěn)定性一般高于 π ,而 π 又高于 δ 。
|
| 上一篇:鍵價(jià)理論的基本知識要點(diǎn) | 下一篇:共價(jià)鍵是否具有方向性 |
|---|
無法在這個(gè)位置找到: xy/left.htm
首 頁 |
對照品|
標(biāo)準(zhǔn)品|
標(biāo)準(zhǔn)物質(zhì)|
實(shí)驗(yàn)試劑|
培養(yǎng)基|
菌種購買|
新聞中心|
聯(lián)系我們|
網(wǎng)站地圖
2011-2018 北京萊耀生物版權(quán)所有豫ICP備17046142號
