查詢時請注意選擇相應的產品編號
| 化學元素周期表的說明和審查 | |||
|---|---|---|---|
|
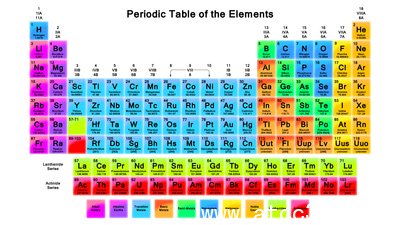
在化學元素周期表中的一個重要工具。這些筆記復習的周期表,它是如何組織的,和元素周期表趨勢的。
周期表中的發明和組織1869年,門捷列夫組織成元素周期表的化學元素,就像我們今天使用的,除責令他的元素按照原子量增加,而現代表增加原子序數組織。元素組成的方式,使得它可以看元素屬性的趨勢,并預測在化學反應中的行為的元素。
排(從左至右)被稱為周期。在一段時間內的元素共享相同的能量水平最高的為未激發電子。有是更多的能級每個原子大小的增加能量水平,所以有更多的元素在周期表進一步回落。
列(從上到下移動)形成的基礎元件組。組中的元素共享相同數目的價電子或外層電子層排布,這給元素組中的一些通用屬性。元素組的例子是堿金屬和惰性氣體。
周期表中的趨勢或周期周期表中的組織使得人們有可能看到的元素的屬性的趨勢一目了然。最重要的發展趨勢與原子半徑,電離能,電負性,電子親和。
原子半徑:原子半徑反映原子的大小。原子半徑減小移動從左至右橫跨一段下跌元素組從上到下增加。雖然也許你認為原子只會變得更大,因為他們獲得了更多的電子,電子留在一個空殼,而越來越多的質子在接近細胞核拉彈。向下移動一組時,電子被進一步從細胞核在新能源彈,所以原子的整體尺寸增加。
電離能是從在氣體狀態下的離子或原子中移走一個電子所需的能量。電離能增加在周期中從左至右移動,并減小移動從上到下向下一個組。
電負性是衡量一個原子形成化學鍵是多么容易。較高的電負性,較高的吸引力用于粘接的電子。電負性減小向下移動一個單元組。對左側的元素周期表的第傾向于是正電性或捐贈一個電子,而不是接受一個更容易。
電子親合反映容易原子接受電子。電子親和能根據不同的元素組。惰性氣體的電子親和,因為他們已經接近零填補電子層。鹵素有高的電子親和能,因為另外的電子給一個原子一個完全充滿的電子層。
|
| 上一篇:化學鍵的類型兩種主要類型的化學鍵離子鍵和共 | 下一篇:原子和分子結構標識它的元素和它的質子數 |
|---|
無法在這個位置找到: xy/left.htm
