查詢時請注意選擇相應的產品編號
| 氫氧化鈉naoh標準溶液的配制與標定實驗報告 | |||
|---|---|---|---|
|
做這個實驗的主要目的 有3個:1、要掌握氫氧化鈉滴定液的配制和標定方法。 2、鞏固用遞減法稱量固體物質。 3、熟悉滴定操作并掌握滴定終點的判斷。 實驗中需要使用到的儀器與試劑 儀器:分析天平、臺秤、滴定管(50mL)、玻棒、量筒、試劑瓶(1000mL)、電爐、表面皿、稱量瓶、錐形瓶 試劑:固體NaOH、基準鄰苯二甲酸氫鉀、純化水、酚酞指示劑
實驗的基本原理與方法 NaOH易吸收空氣中CO2而生成Na2CO3,反應式為: 2NaOH + CO2 = Na2CO3 + H2O 由于Na2CO3在飽和NaOH溶液中不溶解,因此將NaOH制成飽和溶液,其含量約52%(w/w),相對密度為1.56。待Na2CO3沉待淀后,量取一定量的上清液,稀釋至一定體積,即可。用來配制NaOH的純化水,應加熱煮沸放冷,除去水中CO2。 標定NaOH的基準物質有草酸(H2C2O4·2H2O)、苯甲酸(C7H6O2)、鄰苯二甲酸氫鉀(KH C8H4O4)等。通常用鄰苯二甲酸氫鉀標定NaOH滴定液,標定反應如下: 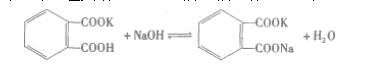
計量點時,生成的弱酸強堿鹽水解,溶液為堿性,采用酚酞作指示劑。按下式計算NaOH滴定液的濃度:
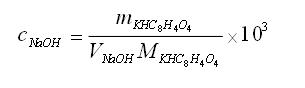 實驗內容 1、NaOH溶液的配制 (1)NaOH飽和溶液的配制:用臺稱稱取120g NaOH固體,倒入裝有100mL純水的燒杯中,攪拌使之溶解成飽和溶液。貯于塑料瓶中,靜置數日,澄清后備用。 (2)NaOH滴定溶液的配制(0.1mol/L):取澄清的飽和NaOH溶液2.8mL,置于1000 mL試劑瓶中,加新煮沸的冷純化水500 mL,搖勻密塞,貼上標簽,備用。 2、NaOH溶液的標定 用遞減法精密稱取在105~110℃干燥至恒重的基準物鄰苯二甲酸氫鉀3份,每份約0.5g,分別置于250 mL錐形瓶中,各加純化水50 mL,使之完全溶解。加酚酞指示劑2滴,用待標定的NaOH溶液滴定至溶液呈淡紅色,且30秒不褪色,即可。平行測定三次,根據消耗NaOH溶液的體積,計算滴定液NaOH的濃度和相對平均偏差。數據記錄與處理 1. 記錄遞減法稱取基準物鄰苯二甲酸氫鉀的質量。 2. 記錄消耗NaOH滴定液的體積。 3. 計算的NaOH濃度及所標定濃度的相對平均偏差 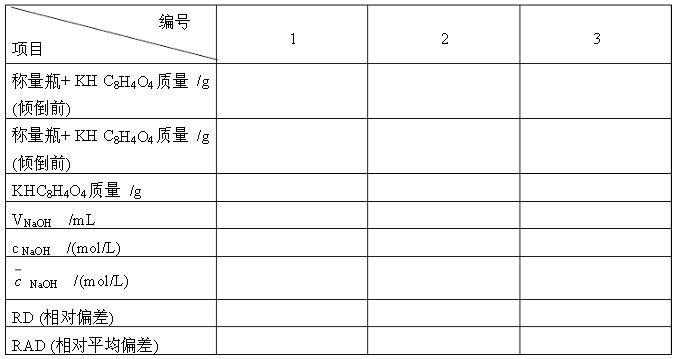 注意事項:1、固體氫氧化鈉應放在表面皿上或小燒杯中稱量,不能在稱量紙上稱量,因為氫氧化鈉極易吸潮。?因而稱量速度盡量快?2、滴定前,應檢查橡皮管內和滴定管尖處是否有氣泡,如有氣泡應排除。否則影響其讀數,會給測定帶來誤差。3、盛放基準物的3個錐形瓶應編號,以免混淆。防止過失誤差。誤差分析等
下面還有幾個氫氧化鈉標準溶液的配制與標定的幾種方法供大家參考:
一、110/(110+100)=52%既然是飽和溶液,必然有沉淀,何況100ml水溶解不了110克的氫氧化鈉,氫氧化鈉在常溫下的溶解度大約是63%,上述等式不成立。正因為是63%的溶解度,57ml的氫氧化鈉飽和溶液含氫氧化鈉溶質接近40克,把57ml的飽和溶液稀釋至1000ml不正好是接近1mol/l的濃度嗎?要確定它的濃度當然要標定了,用苯二甲酸氫鉀標定即可。之所以采取飽和溶液的方式來配制而不采取直接稱取氫氧化鈉固體的方式配制溶液在于,氫氧化鈉中含的碳酸鈉、碳酸氫鈉的溶解度比氫氧化鈉的溶解度小,在飽和溶液中沉淀。這樣,從上層取的氫氧化鈉飽和溶液品質就高,不含碳酸鈉等雜質。
二、1、先通過你想要的溶液體積和濃度所需要NaoH的大概質量,在托盤天平上稱量即可,然后通過間接法配置NaoH溶液(先要將固體NaoH放入燒杯用少量水溶解NaoH,然后加蒸餾水至你想要的體積即可,此過程不需要精確的配置)。2、用已知濃度的HCl溶液標定NaoH溶液:將NaoH溶液置于堿式滴定管中,取一定體積的HCl溶液與錐形瓶中,加入幾滴酚酞做指示劑,然后即可開始滴定,滴定至溶液顯淺紅色為止即可,然后記錄消耗NaoH溶液的體積。3、將NaoH溶液裝到滴定管和第一次大致一樣的高度,重復上述操作,一般平行三次實驗即可
三、1.先配制氫氧化鈉的飽和溶液,一般要放置一周后再取上層清洗用。2.需用煮沸去二氧化碳的水,冷卻過程中需隔絕空氣或者有吸收二氧化碳的裝置。3.計算加入氫氧化鈉的體積。搖勻。4.初步標定,濃度是否在要求范圍內,不符合加水或加氫氧化鈉。5.標定。一般五平行,兩人同標。誤差符合要求后取平均值。(標定用鄰苯二甲酸氫鉀基準試劑,需烘干處理。)注意在配置、標定、貯存過程中均需要防止吸收二氧化碳。
|
| 上一篇:實驗中的化學試劑最常見物質鑒別方法 | 下一篇:淀粉是什么做的工業級淀粉的作用以及用途 |
|---|
無法在這個位置找到: xy/left.htm
